共同决策与哮喘管理
2018/02/12
四川大学华西医院中西医结合科呼吸组 610041
支气管哮喘(简称哮喘)是世界范围的公共健康问题。我国新近的数据显示,北京和上海的哮喘发病率分别较10年前增加了147.9%和190.2%[1],罹患哮喘的绝对人数约3000万[2]。尽管给予吸入糖皮质激素(ICs)/长效β2受体激动剂(LABA)为主的联合治疗策略,可使达到完全控制的哮喘比例得到极大提高[3],但真实世界的研究表明,仍有相当比例的哮喘患者未得到完全控制[4]。而且,与世界其他国家比较,我国哮喘死亡率居世界首位,逾50%的患者曾在过去1年内因哮喘急性发作住院或急诊[2]。哮喘控制不佳严重影响生活质量,甚至危及生命[5]。
一、哮喘控制与依从性
基于全球哮喘防治创议(Global Initiative for Asthma ,简称GINA)和我国哮喘诊治指南,绝大多数哮喘患者规律使用ICs或ICs/LABA能获得并维持哮喘控制。尽管哮喘患者经教育可正确使用ICs或ICs/LABA,但真实世界的研究结果显示哮喘患者对于控制药物的非依从性高达10%-46%[6]。较差的依从性不能持续有效地抑制气道炎症,导致哮喘控制不佳、功能受限、生活质量降低[7],增加住院甚或死亡[8],显然治疗依从性在维持哮喘控制中起着重要作用。依从性差至少表明,目前的哮喘管理计划可能不为患者所接受[6]。从患者角度考虑,或许医生给予的治疗计划不能帮助自身达到预设目标,或者基于其他原因,患者难以遵从医嘱。随着生物-医学-社会医疗模式的转变,以患者为中心的诊疗模式越来越受到重视,如何提高哮喘患者的依从性,提高哮喘控制水平是一个亟需解决的问题。
二、共同决策
以患者为中心的诊疗模式,是指“尊重和回应患者个人偏好、需求和价值观,并确保患者价值观指导所有临床决策的医疗模式”[9]。而共同决策(shared decision-making,SDM)是以患者为中心的诊疗模式的一部分,是美国医学研究所(Institute of Medicine,IOM)评判高质量医疗服务的关键要素[10]。共同决策于1982年被美国医学、生物医学与行为伦理委员会首次提出,描述相互尊重和伙伴关系的过程,旨在帮助患者接受他们偏好的治疗[11]。共同决策被视为通过增加患者对疾病的了解和自主感,或增加患者治疗决策的参与度,来减少医生和患者间的信息不对称[12, 13]。在临床中,共同决策涉及患者和医生之间的相互作用以及信息共享,医生帮助患者了解其面临决策的医学证据,患者帮助医生了解他们对这些决策的需求、价值观和偏好。其后,医生和患者共同做出与医学科学一致的、个性化的诊疗计划[13]。简单地说,共同决策是临床医生和患者应用最佳可靠证据共同做出决策的一种模式(如图1所示),它促进临床医生和患者间的积极的双向参与性协作。
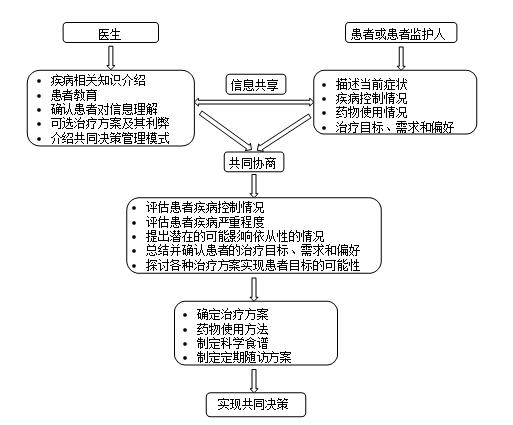
Charles等[12, 13]指出共同决策的标准及特征主要包括:
(1)共同决策涉及至少两个参与者,即医生和患者(或患者监护人)。如果只由一方来做决策,那么这种模式不属于共同决策。由于诊断产生的压力,不确定的结果,以及疾病发展和治疗管理对其他家庭成员的潜在影响,家庭成员亦可能参与治疗决策,而且家庭成员参与诊治决策的讨论,对于某些严重疾病可能特别重要。
(2)医生和患者共同参与诊治决策过程。对医生而言,需要介绍可行的临床选择及其相关的优点、风险和成本,药物使用方法及不良反应等[14]。对患者而言,必须参与决策过程,包括诉说自身的价值观和偏好,以及接受医生的教育、与医生共同讨论,衡量和评估其他治疗方案[11, 13],以确保患者对不同方案的理解和各种方案实现患者目标的可能性等。
(3)信息共享是共同决策的先决条件。在共同决策中,信息共享是第一步,信息的交流是双向的,信息传递的方向和信息传递量亦会因为医生和患者对于疾病理解度之间的差异而发生变化。由于医生和患者之间信息不对等,共同决策模式会花费更多时间,并且医患之间需要建立信任,只有在相互信任的基础上,共同决策模式才可能得以实施。
(4)双方共同作出并同意治疗决策,即患者和临床医生一起讨论和评估治疗选择,建立关于治疗的共识。“共同决策”强调共同接受,双方对于最终决策均需分担责任。共同决策能够充分考虑患者在疾病治疗中的主导地位,是医生对患者的个人偏好、需求和价值做出反应的治疗,并确保患者价值观指导所有临床决策。
三、共同决策与哮喘管理
未能考虑患者个体状况、目标及其偏好可能会降低患者依从性[15]。事实上,GINA和我国的哮喘指南已包含共同决策的要素。例如临床决策需考虑患者和临床医生的目标和偏好,要求患者不仅参与哮喘管理和治疗,而且要参与治疗决策本身的制定[11]。罹患慢病(包括哮喘)的患者依从性差,会限制基于个体和群体患者既定疗法的有效性,并且可能丧失减少不良事件、改善健康的机会[16]。共同决策可能在慢病(如哮喘)管理中起重要作用,其中患者需要改变其生活方式并进行定期评估和决策。患者积极参与决策制定,其坚持治疗方案的可能性会增加。因此,在治疗和管理哮喘等慢性疾病时,共同决策具有道德层面的必要性(即认识到患者在治疗中有发声的权利)和实际的理由(practical rationale)(即认识到非药物治疗的重要性)[11]。证据表明共同决策管理模式对高血压的管理产生了积极的影响[17]。共同决策管理模式能够提高患者在医疗活动中的参与度、促进血压的良好控制,这是独立于药物依从性而起作用的[18]。并且发现在积极参与共同决策管理模式的患者中,收缩压的控制更好[19]。尽管共同决策尚未广泛应用,但对哮喘管理的效应已初步产生显著的积极意义。
1、依从性
一项探讨哮喘患者依从性影响因素的调查显示,哮喘患者希望更多地参与治疗方案的制定,表明共同决策管理模式为哮喘患者所接受[20]。另一项横断面调查发现,哮喘患者参与决策的愿望越大,其对药物治疗的非依从性(Non-compliance)的可能亦越大,此表明未能考虑患者的参与愿望可能会导致依从性降低[21]。一项包含808例女性哮喘患者的队列研究[22],探索了应用共同决策管理模式对哮喘结局的影响。该研究通过电话随访,记录患者在基线、1年和2年后的依从性和哮喘控制情况。结果发现,参与共同决策的患者的依从性是未参与组患者的2.41倍,且共同决策可明显减少因哮喘急性发作需要口服激素的风险(OR=0.21, 95%CI=[0.05, 0.93])。
另一项为期2年的队列研究[23],通过电话随访324例女性哮喘患者在基线、12月和24月末是否参与共同决策以及参与次数,探索共同决策管理模式对患者治疗方案依从性以及治疗满意度的影响。结果显示,38%的受访者在3个时间点都参与了共同决策(A组),36%的受访者只参与了1次(B组),而25%的受访者没有参与过共同决策(C组)。以全程参与共同决策的A组比较,在校正家庭收入,哮喘控制水平等因素后,B组和C组患者的依从性分别为A组的30%和28%。此外,未参与共同决策与治疗满意度成负相关(回归系数(regression coefficient)=-0.65,标准误(sx)=0.17,P<0.001);相反,全程参与共同决策的患者对哮喘治疗方案具有更好的依从性和更高的满意度。此项研究探索了共同决策管理模式对哮喘患者依从性和治疗满意度的影响,对未来的研究和临床实践均有潜在意义。
一项包含612例控制不佳哮喘患者为期2年的多中心随机对照临床试验[24],亦提供了共同决策管理模式能提高哮喘患者依从性的证据。该研究采用随机分配将患者分为三组,分别接受(1)共同决策(SDM),包括评估患者的哮喘控制水平,对患者进行教育,讨论患者的目标和偏好,根据患者的目标和偏好确定治疗方案,以便达到患者和医生彼此可接受的治疗决策; (2)临床医生决策(clinical decision making,CDM),包括与共同决策相同的哮喘控制水平的评估和提供哮喘患者相同的教育,但不考虑患者的目标和偏好,仅由临床医生建议治疗方法。(3)常规治疗(Usual Care,UC),即基于长期哮喘控制目标进行药物治疗的分阶段保健方法,其中允许卫生专业人员(非医生)提供哮喘教育,并以与临床医生决策相似但结构较差的方式解决依从性、药物使用和自我管理的问题。然后比较三组患者药物的依从性和临床结果间的差异。
该研究采用两种方式评估药物的依从性:
(1)连续药物获取指数(continuous medication acquisition ,CMA),即患者每年使用药物的总天数除以365;
(2)倍氯米松(beclomethasone)当量,是1年内患者获得的哮喘控制药物相当于(即在其抗炎强度方面是等效的)倍氯米松(80微克)的总罐数。将患者在1年中所有控制药物加权值相加,以获得控制药物剂量的累积量。结果显示,在1年末,与UC组(CMA=0.46,P<0.0001)和CDM组(CMA=0.59,P=0.029)比较,SDM组(CMA=0.67)的患者对控制药物具有依从性的可能性更高。类似地,如果以倍氯米松当量(单位:罐)来评价患者对哮喘治疗方案依从性时,SDM组具有依从性的可能性是UC组(10.9 vs 5.2; P<0.0001)的两倍以上,并且数值上高于CDM组(10.9 vs 9.1; P=0.005)。同样,比较三组患者在吸入糖皮质激素(ICs)的差异时,SDM组(CMA=0.59)明显高于UC组(CMA=0.37; P<0.0001)和CDM组(CMA=0.52; P=0.017),而且SDM组LABA连续药物获取指数(CMA=0.51)亦显著高于UC组(CMA=0.40;P=0.0225)和CDM组(CMA=0.41; P=0.0143),在第2年末亦观察到类似的结果,即SDM组的LABA用量(CMA=0.52)显著高于UC组(CMA=0.42; P=0.0296)和CDM组(CMA=0.43; P=0.0346)。可见共同决策组的患者在累积控制药物、吸入糖皮质激素(ICs)和长效β受体激动剂(LABA)的使用具有更好的依从性。由此推断参与共同决策的患者比接受常规治疗管理(临床医生起决定作用的治疗方案)的患者,更有可能遵循吸入糖皮质激素(ICs)和其他控制药物包括长效β受体激动剂(LABA)的治疗。
2、哮喘控制
Wilson等[24]的研究亦探讨了共同决策管理模式对哮喘控制的影响。在第1年末的随访中,采用哮喘治疗评估问卷(Asthma Therapy Assessment Questionnaire;ATAQ)评估三组患者的哮喘控制情况,结果显示三组患者的ATAQ评分都较基线时有所改善,其中SDM组降低了0.8分,CDM组降低了0.54分,而UC组降低了0.46分。并且SDM组中自我报告哮喘完全控制(即ATAQ=0)的患者大约是UC组的两倍(OR=1.9;95%CI = [1.3,2.9];P=0.002),但与CDM组比较没有显著性差异(P=0.42)。采用5条目哮喘生活质量评分(The five-item Mini Asthma Quality of Life Questionnaire,mAQLQ)结果显示,SDM组(mAQLQ =5.5)明显高于UC组(mAQLQ =5.1,P=0.0003),且在基线时,与UC组(55.6%)和CDM组(61.1%)相比,有70.3%的SDM组患者的mAQLQ评分提高了至少0.5分。就缓解药物而言,SDM组患者(校正后的沙丁胺醇当量=6.5)使用缓解药物的量显著低于UC组(校正后的沙丁胺醇当量=8.1;P=0.002),数值上亦低于CDM组(校正后的沙丁胺醇当量=7.1;P =0.19)。SDM组的FEV1%校正后平均百分比为76.5%明显高于UC组(73.1%;P=0.0068),同样数值上亦高于CDM组(75.8%;P=0.47)。就哮喘远期风险,SDM组因哮喘急诊就诊率(平均为1.0次/每年)明显低于常规治疗组(1.4次/每年; P=0.0161)。在第二年的随访中,三组患者的急救药物使用量都较第一年末减少,同样SDM组患者(校正后的沙丁胺醇当量=4.7)急救药物使用量显著低于UC组((校正后的沙丁胺醇当量=6.3; P=0.0141),同样也低于CDM组(校正后的沙丁胺醇当量=6.0; P= 0.06)。显然,参与共同决策的患者与接受常规治疗的患者相比,在哮喘控制水平、哮喘相关生活质量,缓解药物使用、肺功能改善,哮喘急性发作远期风险等方面具有显著优势,并且在数值上亦优于临床决策组。虽然SDM组与CDM组相比,基于有限的样本量,二者的临床结果差异并未显示统计学差异,但客观测量指标和患者自我报告结果均倾向于SDM组的改善更大。因此,我们认为共同决策可有效提高哮喘患者的临床结局。
一项由746名儿童哮喘患者参与的前瞻性队列研究[25],探索了在真实世界中,共同决策对儿童哮喘患者在急诊、住院、口服激素等远期临床结局方面的影响。该研究分为干预组(共同决策组)和对照组(常规治疗组),分别在基线、3月、6月和12月末对患者进行随访。结果显示,共同决策组(33%)在1年内的哮喘急性加重次数(定义为哮喘相关的急诊、住院或口服糖皮质激素)比常规治疗组(47%,P = 0.023)显著减少。
然而Noreen M. Clark等[22]的研究显示:参与共同决策的患者具有更频繁的日间(17%,95%CI = [8%,27%])和夜间(31%,95%CI = [16%,48%])症状。作者猜测虽然参与共同决策患者和对照组患者的症状报告在基线时没有差异,但前者可能包含更多在哮喘阶梯治疗中处于较高级别的患者,如需要更多的哮喘处方药,口服糖皮质激素的患者比例更多等,这可能是参与共同决策患者具有更多症状的一个原因。
3、医疗花费和经济负担
近年来,共同决策被期望作为一种策略,用于减少过度治疗和医疗花费。理论上认为,由于医患之间充分沟通、疾病信息对等,患者过度医疗的可能性会降低,医疗花销和经济负担随之减少。据the Lewin Group估计,从1997年到2008年,共同决策管理模式实施的11年多以来,美国的医疗花费降低了90多亿美元[26]。此外,华盛顿健康组织2012年的一项研究显示,为符合髋、膝关节置换术的患者提供共同决策,大大降低了手术率和医疗花销:其中手术率降低了38%,6个月的医疗花销降低了12%-21%[27]。但是在哮喘管理中,共同决策与医疗花费和经济负担的关系还不是很明确。
一项由10个研究中心,至少500名患者参与的多中心随机临床试验研究显示,参与共同决策的中心,其哮喘恶化(即急诊就诊或住院)患者的比例从16%下降到9%[28]。同样,Minal R. Patel[23]等的研究结果显示,与全程参与了共同决策的患者相比,参与共同决策不足三次的患者,具有更高的急诊就诊率(OR = 1.37,95%CI=[1.07,1.61];P<0.01),即是说参与共同决策不足三次的患者相对于全程参与了共同决策的患者而言,急诊就诊的风险比是1.37,但未观察到住院率和哮喘症状之间的差异。再者Noreen Clark等[22]研究显示共同决策对于哮喘患者的住院率(OR=0.99,95%CI=[0.63,1.55];P=0.95),急诊率(OR=1.02,95%CI=[0.89,1.17];P=0.77)和非定期随访率(OR=1.03,95%CI=[0.91,1.17]; P=0.63)之间没有差异,可能需要额外的策略来减少哮喘症状和急性医疗事件的发生。作者解释这样的结果可能是由于观察时间不够,医疗花费的降低可能会在共同决策实施更长的时间段内出现。
四、共同决策的挑战
虽然共同决策被希望用于慢病的长期管理,似乎得到了患者和临床医生的一致认可,但目前最大的挑战是如何更好地使共同决策在临床实践中成为现实[29]。临床医生如果没有经过共同决策的充分培训,特别是如何引出患者的价值和偏好,对共同决策如何实施不熟悉,那么共同决策管理模式很难实施[28]。再者,患者因素如健康素养,教育程度和对医疗保健资源的获取能力亦构成重大挑战,患者参与决策的偏好差异很大,对于如何将不同参与意愿纳入决策知之甚少[30]。其次,完成共同决策所需的时间亦可能成为一个挑战。最近由Legaré等进行的一次研究发现,平均完成共同决策所需要的时间是23分钟[31]。特别是在医疗资源有限的地区,过多的时间花费可能是实施共同决策难以逾越的障碍。同样共同决策的实施,亦面临着财政压力:医疗保健预算往往不会为临床医生提供教育患者的额外资助;结构化的医疗过程可能通过限制可用治疗方案的选择成为共同决策的附加障碍。例如,在具体的医疗保险结构中,患者可能只有有限的治疗方案可供选择。在这些情况下,由于治疗方案的有限,患者的价值和偏好不能被充分考虑,而背离了共同决策管理的初衷。
五、结语
尽管共同决策存在潜在的好处,但在临床实践中尚未广泛实施。共同决策管理模式有助于哮喘患者的自我管理,提高患者的依从性,但仍缺乏足够的证据表明共同决策会改善患者结局,降低医疗花费和经济负担,在临床应用中难免会显得证据不足,很少有研究提供证据表明严格测试的共同决策模型/干预能够运用于临床医疗活动中,特别是共同决策在哮喘管理中的应用[32]。同样尚没有研究探索共同决策实施成本和效益之间的关系。迫切需要更多的研究来探索在真实世界中共同决策的实施指南,并研究共同决策是如何影响治疗依从性和临床结果的机制。
参考文献
[1] 苏楠,林江涛,刘国梁,等. 我国8省市支气管哮喘患者控制水平的流行病学调查[J]. 中华内科杂志,2014,53(8):601-606.
[2] Su N, Lin J, Chen P, et al. Evaluation of asthma control and patient's perception of asthma: findings and analysis of a nationwide questionnaire-based survey in China[J]. J Asthma,2013,50(8):861-870. PMID: 23713625
[3] Bateman E D, Boushey H A, Bousquet J, et al. Can guideline-defined asthma control be achieved? The Gaining Optimal Asthma ControL study[J]. Am J Respir Crit Care Med,2004,170(8):836-844.PMID: 15256389
[4] Papaioannou A I, Kostikas K, Zervas E, et al. Control of asthma in real life: still a valuable goal?[J]. Eur Respir Rev,2015,24(136):361-369. PMID: 26028647
[5] 苏楠,林江涛,刘国梁,等. 我国八省市支气管哮喘患者对疾病管理与认知现状调查[J]. 中华内科杂志,2015,54(8):680-683.
[6] Juniper E F. The impact of patient compliance on effective asthma management[J]. Curr Opin Pulm Med,2003,9 (Suppl 1):S8-S10. PMID: 12974536
[7] Gillisen A. Patient's adherence in asthma[J]. J Physiol Pharmacol,2007,58 Suppl 5(Pt 1):205-222. PMID: 18204131
[8] Sokol M C, Mcguigan K A, Verbrugge R R, et al. Impact of medication adherence on hospitalization risk and healthcare cost[J]. Med Care,2005,43(6):521-530. PMID: 15908846
[9] Barry M J, Edgman-Levitan S. Shared decision making--pinnacle of patient-centered care[J]. N Engl J Med,2012,366(9):780-781. PMID: 22375967
[10] Kane H L, Halpern M T, Squiers L B, et al. Implementing and evaluating shared decision making in oncology practice[J]. CA Cancer J Clin,2014,64(6):377-388. PMID: 25200391
[11] Rivera-Spoljaric K, Halley M, Wilson S R. Shared clinician-patient decision-making about treatment of pediatric asthma: what do we know and how can we use it?[J]. Curr Opin Allergy Clin Immunol,2014,14(2):161-167. PMID: 24553296
[12] Charles C, Gafni A, Whelan T. Shared decision-making in the medical encounter: what does it mean? (or it takes at least two to tango)[J]. Soc Sci Med,1997,44(5):681-692. PMID: 9032835
[13] Charles C, Gafni A, Whelan T. Decision-making in the physician-patient encounter: revisiting the shared treatment decision-making model[J]. Soc Sci Med,1999,49(5):651-661. PMID: 10452420
[14] Fowler F J, Gallagher P M, Drake K M, et al. Decision dissonance: evaluating an approach to measuring the quality of surgical decision making[J]. Jt Comm J Qual Patient Saf,2013,39(3):136-144. PMID: 23516764
[15] Katz S J, Hawley S. The value of sharing treatment decision making with patients: expecting too much?[J]. JAMA,2013,310(15):1559-1560. PMID: 24061082
[16] Fiks A G, Mayne S L, Karavite D J, et al. Parent-reported outcomes of a shared decision-making portal in asthma: a practice-based RCT[J]. Pediatrics,2015,135(4):e965-e973. PMID: 25755233
[17] Tinsel I, Buchholz A, Vach W, et al. Implementation of shared decision making by physician training to optimise hypertension treatment. Study protocol of a cluster-RCT[J]. BMC Cardiovasc Disord,2012,12:73. PMID: 22966894
[18] Naik A D, Kallen M A, Walder A, et al. Improving hypertension control in diabetes mellitus: the effects of collaborative and proactive health communication[J]. Circulation,2008,117(11):1361-1368. PMID: 18316489
[19] Deinzer A, Babel H, Veelken R, et al. [Shared decision-making with hypertensive patients. Results of an implementation in Germany][J]. Dtsch Med Wochenschr,2006,131(46):2592-2596. PMID: 17096305
[20] Bender B G, Long A, Parasuraman B, et al. Factors influencing patient decisions about the use of asthma controller medication[J]. Ann Allergy Asthma Immunol,2007,98(4):322-328. PMID: 17458427
[21] Schneider A, Wensing M, Quinzler R, et al. Higher preference for participation in treatment decisions is associated with lower medication adherence in asthma patients[J]. Patient Educ Couns,2007,67(1-2):57-62. PMID: 17346917
[22] Clark N M, Ko Y A, Gong Z M, et al. Outcomes associated with a negotiated asthma treatment plan[J]. Chron Respir Dis,2012,9(3):175-182. PMID: 22848067
[23] Patel M R, Valerio M A, Janevic M R, et al. Long-term effects of negotiated treatment plans on self-management behaviors and satisfaction with care among women with asthma[J]. J Asthma,2013,50(1):82-89. PMID: 23189924
[24] Wilson S R, Strub P, Buist A S, et al. Shared treatment decision making improves adherence and outcomes in poorly controlled asthma[J]. Am J Respir Crit Care Med,2010,181(6):566-577. PMID: 20019345
[25] Tapp H, Shade L, Mahabaleshwarkar R, et al. Results from a pragmatic prospective cohort study: Shared decision making improves outcomes for children with asthma[J]. J Asthma,2017,54(4):392-402. PMID: 27813670
[26] Oshima L E, Emanuel E J. Shared decision making to improve care and reduce costs[J]. N Engl J Med,2013,368(1):6-8. PMID: 23281971
[27] Arterburn D, Wellman R, Westbrook E, et al. Introducing decision aids at Group Health was linked to sharply lower hip and knee surgery rates and costs[J]. Health Aff (Millwood),2012,31(9):2094-2104. PMID: 22949460
[28] Tapp H, Mcwilliams A, Ludden T, et al. Comparing traditional and participatory dissemination of a shared decision making intervention (ADAPT-NC): a cluster randomized trial[J]. Implement Sci,2014,9:158. PMID: 25359128
[29] Pollard S, Bansback N, Fitzgerld J M, et al. The burden of nonadherence among adults with asthma: a role for shared decision-making[J]. Allergy,2017,72(5):705-712. PMID: 27873330
[30] Kambhampati S, Ashvetiya T, Stone N J, et al. Shared Decision-Making and Patient Empowerment in Preventive Cardiology[J]. Curr Cardiol Rep,2016,18(5):49. PMID: 27098670
[31] Pollard S, Bansback N, Fitzgerld J M, et al. The burden of nonadherence among adults with asthma: a role for shared decision-making[J]. Allergy,2017,72(5):705-712. PMID: 27873330
[32] Upton J, Fletcher M, Madoc-Sutton H, et al. Shared decision making or paternalism in nursing consultations? A qualitative study of primary care asthma nurses' views on sharing decisions with patients regarding inhaler device selection[J]. Health Expect,2011,14(4):374-382. PMID: 21323822
上一篇:
大环内酯类药物在中性粒细胞型哮喘中的治疗作用
下一篇:
奥马珠单抗-开启中重度过敏性哮喘治疗新篇章









