- 注册时间
- 2007-3-15
- 最后登录
- 2024-5-8
- 在线时间
- 443 小时
- 阅读权限
- 150
- 积分
- 19740
- 帖子
- 542
- 精华
- 1
- UID
- 128
 
|
本帖最后由 wjh 于 2021-9-16 10:59 编辑
胡群 吴雯雯 姬郁林 王刚
四川大学华西医院呼吸与危重症医学科(四川成都 610041)
支气管哮喘(简称哮喘)是一种以慢性气道炎症为特征的异质性疾病,以随时间变化的喘息、气促、胸闷或咳嗽为表现,并有不同程度的呼气气流受限[1]。重症哮喘占所有哮喘患者的5%~10%,定义为即使使用全球哮喘防治创议(GINA)第4~5级阶梯治疗哮喘仍未控制,或是需要GINA第4、5级阶梯治疗以维持良好的症状控制和减少即存在的急性发作风险[1]。重症哮喘的管理方式十分复杂。Irwin等[2]于1993年首次提出重症哮喘的多维度评估,即至少包括气道病理、共患疾病、危险因素、自我管理技能中两方面评估内容[3],并证明此评估方法对患者健康及预后有益。近年Gibson等[4]和Agusti等[5]再次提到,对复杂气道慢性疾病而言,多维度评估可使我们对疾病有更全面、更深入的理解,从而识别出可治疗特质(treatable traits),即包括疾病表型(phenotype)和内型(endotype)等特征,以对此进行针对性、个体化治疗,更益于疾病管理。
参考文献并结合临床实践,我们建立了适合自己的重症哮喘多维度评估模型(图1)。本文旨在系统阐述在重症哮喘中运用该模型识别患者的可治疗特质,以期改善患者健康状况。
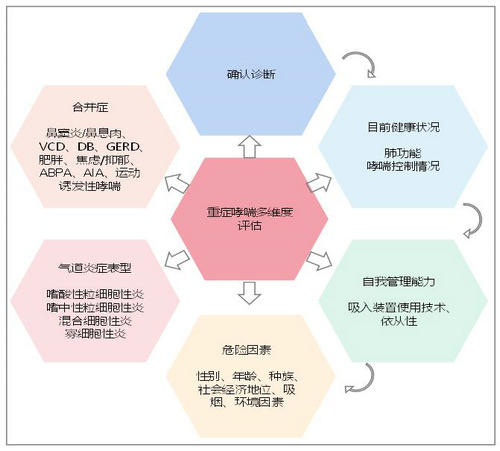
图1 重症哮喘的多维度评估模型
VCD:声带功能异常;DB:呼吸功能失调;GERD:胃食管反流;ABPA:变应性支气管肺曲菌病;AIA:阿司匹林哮喘
1、确认诊断
确定哮喘的诊断是治疗和评估哮喘的前提。哮喘症状具有非特异性、多样性和复杂性,同时受到多种因素的影响,哮喘的误诊率很高[6]。根据GINA制定的诊断标准[1]和我国新版支气管哮喘防治指南的观点[7],哮喘的诊断需要有可变的呼吸道症状病史和可变的呼气气流受限证据。
2、目前健康状况评估
患者目前健康状况包括肺功能及哮喘控制情况。肺功能测试(表1)包括但不限于气流受限、气道高反应性及气道可逆性评估,目的在于明确患者是否存在上述情况及其程度[8]。重症哮喘中第一秒用力呼气容积(FEV1)基础值更低可能提示对大剂量吸入性激素(ICS)治疗的反应性更好[9]。哮喘控制情况及其生活质量可采用一些简单、便捷、有效的症状问卷量表,包括哮喘控制问卷(ACQ)、哮喘控制测试(ACT)、哮喘生活质量问卷(AQLQ)等[10-12]。较差的哮喘控制与未来急性发作的风险相关[13]。

3、自我管理能力评估
依从性差及吸入装置使用技术不足,是患者自我管理中引起哮喘控制差的最常见的因素[2]。在重症哮喘患者中,无论是成人或儿童对治疗的依从性往往都很差,其比例超过50%[14]。不足的自我管理能力与重症哮喘急性发作风险显著相关[15],因此,对于依从性差且吸入用药装置技术不足的患者,对其进行吸入用药装置宣教并加强用药监督,如制定哮喘行动计划,可使患者自我管理能力得到改善,从而提高健康相关生活质量并降低未来急性发作风险。
4、危险因素评估
哮喘诱发因素的可变性很大,并且可能随着时间的变化而改变,这与暴露(药物、食物[2]、季节性过敏)有关,还受到其他环境因素的影响,包括湿度、温度和颗粒物[16,17]。同样,接触香烟烟雾亦是诱发哮喘的重要危险因素,是哮喘症状控制和哮喘严重程度的独立危险因素,不仅与急性发作风险有关,还可能降低呼出气一氧化氮水平,削弱患者对激素治疗的反应性[9,18,19]。此外,哮喘急性发作的危险因素还包括性别、年龄、种族、社会经济地位和呼吸道病毒的暴露[20],但一项表型明确、多中心、不同年龄重症哮喘队列研究显示,频繁急性发作型哮喘与哮喘的持续时间、发病年龄、种族和社会经济地位没有相关性,只有在成人患者中,急性发作的频率才与年龄有关,且频繁急性发作的患者年龄更大[21]。
5、气道炎症表型评估
《重症哮喘诊断与处理中国专家共识》[22]根据患者发病年龄等状态将重症哮喘的临床表型分为早发过敏性哮喘、晚发持续嗜酸粒细胞炎症性哮喘、频繁急性发作性哮喘、持续气流受限性哮喘、肥胖相关性哮喘,各型有不同的临床特征,据此分型可区分患者对激素反应性而指导个体化治疗。根据诱导痰细胞计数,重症哮喘气道炎症表型可分为以下四种:(1)嗜酸性粒细胞性哮喘:痰嗜酸性粒细胞百分比≥ 3%;(2)中性粒细胞性哮喘:痰中性粒细胞百分比≥ 61%;(3)混合性粒细胞性哮喘:痰嗜酸性粒细胞百分比≥ 3%,且中性粒细胞百分比≥ 61%;(4)寡粒细胞性哮喘:痰嗜酸性粒细胞和中性粒细胞百分比正常[23]。将重症哮喘根据气道炎症分型可针对不同气道炎症表型指导重症哮喘治疗。
嗜酸性粒细胞性炎症表型在重症哮喘患者中比例较大[24],根据痰嗜酸粒细胞水平调整治疗方案,不仅可降低哮喘患者急性发作风险,评估气流阻塞和支气管高反应性,还可减小ICS用药剂量[25,26]。嗜酸粒细胞哮喘的分子机制涉及2型T辅助细胞(Th2)或高T2型(Type-2 high)炎症,其特征为气道上皮细胞暴露于Th2型细胞因子(白细胞介素中的IL-4、IL-5、IL-13)等炎症介质下所刺激的基因表达被广泛识别。IL-4和IL-5分别促进IgE和嗜酸性粒细胞的产生,通常表现为嗜酸粒细胞炎症,这种炎症表型的哮喘患者可能对针对Th2型的生物治疗反应良好,如抗IL-5抗体[27,28]。激素可减轻气道嗜酸性粒细胞的浸润,减少促炎症介质和细胞因子的产生[9],但仍有部分嗜酸粒细胞哮喘患者即使使用大剂量ICS或口服激素仍然效果欠佳,此时可考虑加用生物治疗。2型炎症生物标志物包括血清IgE、血/痰嗜酸粒细胞计数、血清骨膜蛋白(Periostin)和呼出气一氧化氮(FeNO)[29],可预测生物靶向治疗的反应性,但这方面仍需更多研究探索。
中性粒细胞炎症表型与哮喘严重程度、激素不敏感和慢性持续气流阻塞相关,气道中性粒细胞炎症的存在与环境中的非过敏性因素,如臭氧、不溶性颗粒物(PM)、内毒素、烟草烟雾、职业刺激物、呼吸道病毒及细菌感染等有关,此种炎症还可通过中性粒细胞弹性蛋白酶、髓过氧化物酶和基质金属蛋白酶-9促进气道重塑[30,31]。中性粒细胞或寡粒细胞炎症均属于低T2型(Type-2 low),相关病理学机制尚未完全明确,对中性粒细胞炎症表型的重症难治性哮喘患者的治疗仍然面临挑战。
6、共病评估
重症哮喘患者往往合并有其他疾病,若不同时治疗这些共病则会明显影响哮喘控制和生活质量,增加急性发作的风险。参考国内外文献[32-35],根据解剖部位将其分为气道和气道外的合并症;此外,还包括哮喘相关合并症,这些在非哮喘患者中几乎不出现[36]。其流行、诊断和针对性干预措施见表2。


7、采用多维度评估方法识别可治疗特质
“可治疗特质(treatable traits)”策略是一种新的指向精准医学的慢性呼吸道疾病管理策略,提倡以识别患者表达的可治疗特质为基础并进行针对性个体化治疗。可治疗特质是指影响疾病症状或预后的“潜在可修正因素”,通常在肺内领域、肺外领域和社会心理/环境/行为危险因素领域被识别,必须具备临床相关性、可识别性或可测量性以及可治疗性3大特点[37,38]。哮喘表型和内型满足以上特点的属于可治疗特质的范畴。表型反映的是可观察到的特征,包括临床上、功能上、影像学或生物标志物的特征。我们新近的研究发现,73.4%的哮喘患者存在表型重叠(phenotype overlap),而且T2和非T2表型重叠占了47.5%[39]。内型反映的是疾病发病机制涉及的细胞和分子通道,包括复杂的固有免疫和适应性免疫反应系统,并受到宏观和微观环境的调控。内型是从发病机制层面解释疾病,表型是内型作用的结果[40]。目前哮喘可治疗特质的研究主要集中于重症哮喘。因目前尚缺乏国际共识或者指南来定义重症哮喘可治疗特质列表清单及对应的识别标记物,参考现有的相关原始研究,我们总结了重症哮喘拟可治疗特质列表、对应的识别方法和治疗手段[5,15,38,41-43](表3)。
8、总结与展望
哮喘是一种异质性疾病,采用多维度评估方法识别重症哮喘的可治疗特质,主要涉及自我管理能力、危险因素、气道炎症表型和相关的合并症,以实施个体化治疗,可改善哮喘症状、提高健康相关生活质量。尽管大量研究表明,多维度评估可明显改善重症哮喘患者预后,但目前该领域的随机对照试验研究很少,仍然没有专家共识或指南推荐说明哪些特征可用于重症哮喘评估和管理中作为多维度评估方法中的一部分,或者哪些特征需要进行针对性治疗。还需要更多的临床研究来说明此种方法的有效性,建立重症哮喘多维度评估模型,逐渐确立多维评估最佳方法的专家共识。
参考文献
1.Global Initiative for Asthma.Global strategy for asthma management and prevention, 2019. www.ginasthma.org.
2.Irwin RS, Curley FJ, French CL; Difficult-to-control asthma. Contributing factors and outcome of a systematic management protocol. Chest, 1993, 103(6): 1662-1669.
3.Clark VL, Gibson PG, Genn G, et al; Multidimensional assessment of severe asthma: a systematic review and meta-analysis. Respirology, 2017, 22(7): 1262-1275.
4.Gibson PG, McDonald VM, Marks GB; Asthma in older adults. Lancet, 2010, 376(9743): 803-813.
5.Agusti A , Bel E, Thomas M, et al; Treatable traits: toward precision medicine of chronic airway diseases. Eur Respir J, 2016, 47(2): 410-419.
6.MacNeil J, Loves RH, Aaron SD; Addressing the misdiagnosis of asthma in adults: where does it go wrong?. Expert Rev Respir Med, 2016, 10(11): 1187-1198.
7.沈华浩,杜旭菲,应颂敏; 新版中国支气管哮喘防治指南与全球支气管哮喘防治创议的异同. 中华结核和呼吸杂志, 2018, 41(3): 166-168.
8.Majellano EC, Clark VL, Winter NA, et al; Approaches to the assessment of severe asthma: barriers and strategies. J Asthma Allergy, 2019, 12: 235-251.
9.Jang AS, Lee JH, Park SW, et al; Factors influencing the responsiveness to inhaled glucocorticoids of patients with moderate-to-severe asthma. Chest, 2005, 128(3): 1140-1145.
10.Juniper EF, O'Byrne PM, Guyatt GH, et al; Development and validation of a questionnaire to measure asthma control. Eur Respir J, 1999, 14(4): 902-907.
11.Nathan RA, Sorkness CA, Kosinski M, et al; Development of the asthma control test: a survey for assessing asthma control. J Allergy Clin Immunol, 2004, 113(1): 59-65.
12.Juniper EF, Guyatt GH, Ferrie PJ, et al; Measuring quality of life in asthma. Am Rev Respir Dis, 1993, 147(4): 832-838.
13.Kupczyk M, Ten Brinke A, Sterk PJ, et al; Frequent exacerbators-a distinct phenotype of severe asthma. Clin Exp Allergy, 2014, 44(2): 212-221.
14.Chung KF, Wenzel SE, Brozek JL, et al; International ERS/ATS guidelines on definition, evaluation and treatment of severe asthma. Eur Respir J, 2014, 43(2): 343-373.
15.McDonald VM, Clark VL, Cordova-Rivera L, et al; Targeting treatable traits in severe asthma: a randomised controlled trial. Eur Respir J, 2020, 55(3): 1901509.
16.May L, Carim M, Yadav K; Adult asthma exacerbations and environmental triggers: a retrospective review of ED visits using an electronic medical record. Am J Emerg Med, 2011, 29(9): 1074-1082.
17.Zheng XY, Ding H, Jiang LN, et al; Association between air pollutants and asthma emergency room visits and hospital admissions in time series studies: a systematic review and meta-analysis. PLoS One, 2015, 10(9): e0138146.
18.Shaw DE , Sousa AR, Fowler SJ, et al; Clinical and inflammatory characteristics of the European U-BIOPRED adult severe asthma cohort. Eur Respir J, 2015, 46(5): 1308-1321.
19.Bateman ED, Buhl R, O'Byrne PM, et al; Development and validation of a novel risk score for asthma exacerbations: The risk score for exacerbations. J Allergy Clin Immunol, 2015, 135(6): 1457-1464.
20.Ramsahai JM, Hansbro PM, Wark PAB; Mechanisms and management of asthma exacerbations. Am J Respir Crit Care Med, 2019, 199(4): 423-432.
21.Denlinger LC, Phillips BR, Ramratnam S, et al; Inflammatory and comorbid features of patients with severe asthma and frequent exacerbations. Am J Respir Crit Care Med, 2017, 195(3): 302-313.
22.中华医学会呼吸病学分会哮喘学组,中国哮喘联盟; 重症哮喘诊断与处理中国专家共识. 中华结核和呼吸杂志, 2017, 40(11): 813-829.
23.Simpson JL, Phipps S, Baines KJ, et al; Elevated expression of the NLRP3 inflammasome in neutrophilic asthma. Eur Respir J, 2014, 43(4): 1067-1076.
24.张晓岩,林江涛,王文雅,等; 35例重症支气管哮喘患者临床特征和气道炎症表型[J]. 中华内科杂志, 2019, 58(9): 680-684.
25.Green RH, Brightling CE, McKenna S, et al; Asthma exacerbations and sputum eosinophil counts: a randomised controlled trial. Lancet, 2002, 360(9347): 1715-1721.
26.Cowan DC, Taylor DR, Peterson LE, et al; Biomarker-based asthma phenotypes of corticosteroid response. J Allergy Clin Immunol, 2015, 135(4): 877-883.
27.Israel E, Reddel HK; Severe and difficult-to-treat asthma in adults. N Engl J Med, 2017, 377(10): 965-976.
28.Kalchiem-Dekel O, Yao X, Levine SJ; Meeting the challenge of identifying new treatments for type 2-low neutrophilic asthma. Chest, 2020, 157(1): 26-33.
29.Semprini R, Shortt N, Ebmeier S, et al; Change in biomarkers of type-2 inflammation following severe exacerbations of asthma. Thorax, 2019, 74(1): 95-98.
30.Chung KF; Diagnosis and management of severe asthma. Semin Respir Crit Care Med, 2018, 39(1): 91-99.
31.黄茂,吉宁飞,吴超杰; 重症哮喘气道炎症机制的新进展. 中华结核和呼吸杂志, 2017, 40(11): 810-812.
32.Porsbjerg C, Menzies-Gow A; Co-morbidities in severe asthma: clinical impact and management. Respirology, 2017, 22(4): 651-661.
33.杨树升,林丽; 36例阿司匹林哮喘回顾性分析. 中国呼吸与危重监护杂志, 2012, 11(5): 448-451.
34.周瑛,肖平,张有志,等; 阿司匹林哮喘:回顾性分析. 中华哮喘杂志(电子版), 2008, 2(1): 56-59.
35.陈欣,林江涛; 运动诱发性哮喘. 中日友好医院学报, 2000, 14(4): 239-241.
36.Schoettler N, Strek ME; Recent advances in Severe Asthma: From Phenotypes to Personalized Medicine. Chest, 2020, 157(3): 516-528.
37.Mcdonald VM, Fingleton J, Agusti A,et al; Treatable traits: a new paradigm for 21st century management of chronic airway diseases: treatable traits down under international workshop report. Eur Respir J, 2019,53(5):1802058.
38.Shrimanker R, Choo XN, Pavord ID; A new approach to the classification and management of airways diseases:
identification of treatable traits. Clin Sci (Lond), 2017,131(10): 1027-1043.
39.Han YY, Zhang X, Wang J, et al; Multidimensional assessment of asthma identifies clinically relevant phenotype overlap: a cross-sectional study. J Allergy Clin Immunol Pract, 2021,9(1):349-362.
40.Agache I; Severe asthma phenotypes and endotypes. Semin Immunol, 2019, 46: 101301.
41.McDonald VM, Hiles SA, Godbout K, et al; Treatable traits can be identified in a severe asthma registry and predict future exacerbations. Respirology, 2019, 24(1): 37-47.
42.Simpson AJ, Hekking PP, Shaw DE, et al; Treatable traits in the European U-BIOPRED adult asthma cohorts. Allergy, 2019,74(2): 406-411.
43.Tay TR, Hew M; Comorbid "treatable traits" in difficult asthma: current evidence and clinical evaluation. Allergy, 2018,73(7): 1369-1382.
|
|